加快标准制定 助力新技术在医疗器械领域高质量
原标题:加快标准制定 助力新技术在医疗器械领域高质量运用——医用增材制造医疗器械全生命周期质量控制和行业标准建设进展介绍
□韩倩倩王春仁李静莉
当新技术应用到医疗器械研发生产中时,要关注因新技术引发的新风险,应用标准的方法来评估风险、评价产品的安全有效性,尽可能在现有技术条件下消除风险。保障新技术的安全应用至关重要。因此,要科学制定基于新技术研发生产的医疗器械的质量评价标准,使新技术在发展之初便得到标准化工作的支撑。有了标准的支撑,一方面,可以使新技术更好更快地应用于产品制造;另一方面,可以缩短产品的研发、验证、临床应用的总体转化时间。在医疗器械新技术应用领域,我国有望实现国际医疗器械研发制造的弯道超车,所以加强基于新技术研发生产的医疗器械的标准化研究,有助于产品上市前的科学把关、落实前瞻性全生命周期监管和规范产业发展。
增材制造技术应用于医疗器械的研发制造是新技术应用的范例。因增材制造技术涉及数据建模、医工交互、个性化定制等环节,所以产品的全生命周期质量管理尤为重要。2021年3月,国家药品监督管理局、国家标准化管理委员会发布了《关于进一步促进医疗器械标准化工作高质量发展的意见》,鼓励开展增材制造医疗器械领域的标准化工作。
国家药监局于2019年批准组织成立医用增材制造技术医疗器械标准技术归口单位,中国食品药品检定研究院作为归口单位秘书处承担单位,通过开展技术研究和组织标准制定,现阶段已经制定发布国家药监局行业标准两项,预研行业标准提案13项,建立了覆盖全生命周期质量控制环节的医用增材制造技术医疗器械行业标准体系。
行业标准研究先行
奠定产品高质量发展标准化基础
增材制造技术将生物医用材料、工程、数据、医学个性化需求交叉汇融,近年来得以逐步广泛应用。增材制造医疗器械产品类型包括医疗用模型、手术导板、骨科产品、组织修复产品、血管植入物、矫形器具等。现阶段增材制造技术产品获注册证14个,主要代表性产品有作为三类医疗器械管理的增材制造髋关节假体、颈椎融合器、骨盆缺损匹配假体;作为二类医疗器械管理的增材制造骨模型、截骨导板、种植牙定位导板等。已经进入临床研究的代表产品有增材制造纯坦骨科植入物、增材制造镍钛合金骨科植入物和增材制造陶瓷骨科植入物等。增材制造应用于医疗器械的制造具备独特的个性化实现和精密微观结构实现的优势,同时也带来了独有的风险。比如粉末状原材料质控缺乏技术指标,设备验证关键生产环节缺乏规范要求,成品检测方法匮乏等。所以,该领域的发展急需风险分析技术、质量控制技术和标准化工作的指导。
面对技术变革,中国食品药品检定研究院开展了医用增材制造医疗器械的检验技术和标准化技术研究,建立了涵盖原材料、工艺验证、设备、数据传输和风险管理的标准体系,并开展行业标准的制定。
从支撑全生命周期监管的角度出发,中国食品药品检定研究院对涉及产品安全有效的各个环节展开研究,确定了十大关键技术和标准化环节,分别是产品设计、原材料质量控制、医工交互、数据建模、设备参数控制、打印后处理、成品质量控制、临床使用、上市后随访、取出物分析。针对各个环节征集标准立项提案,共预研了13项行业标准提案,其中现阶段已经制定发布了增材制造技术的基础性原材料标准YY/T 1701-2020《用于增材制造的医用Ti-6Al-4V/Ti-6Al-4V ELI粉末》、YY/T 1809-2021《医用增材制造 粉末床熔融成形工艺金属粉末清洗及清洗效果验证方法》,2021年度组织制定了一项关于用于增材制造的医用纯属坦粉末的行业标准。
着眼全生命周期质量控制
构建覆盖全环节的行业标准体系
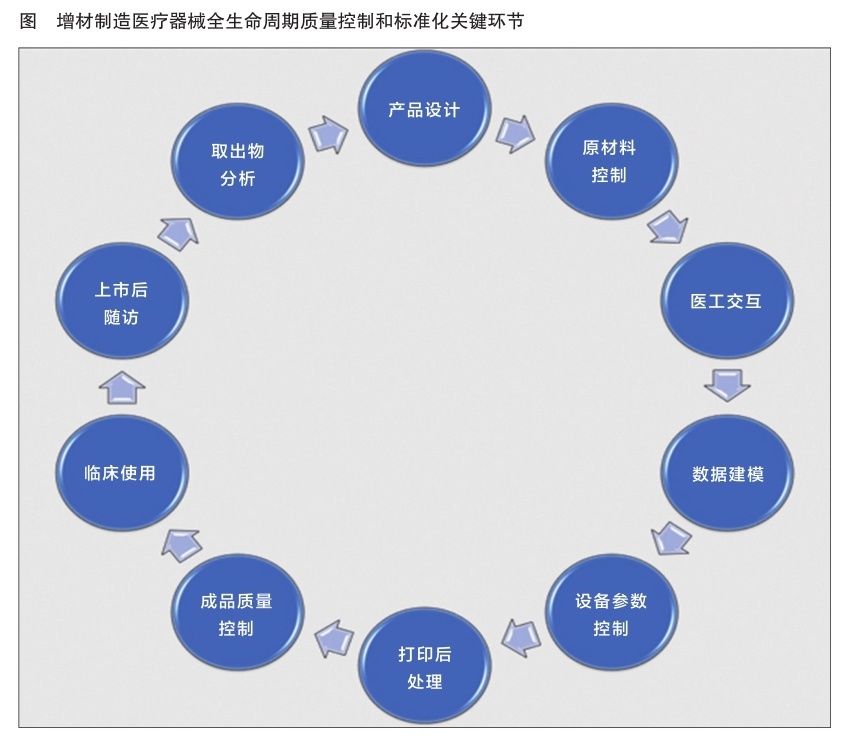
完善的标准是质量可控的重要保障之一。根据增材制造医疗器械的特点,归口单位秘书处研究建立了10个质量控制及标准技术研究环节(详见图)。只有各个环节都做到满分,才能达到成品的质量可控。
产品设计增材制造医疗器械的设计包含外形设计和内部结构设计。增材制造医疗器械的临床应用优势是可以进行个性化定制,即根据患者的特殊病损进行设计。以骨植入类产品为例,可以设计独特的三维精密结构以增加其骨整合性,好的设计可以使骨整合更好、使功能发挥符合患者的个体特点。针对产品设计,现阶段已经有预研标准两项:骨植入物设计流程和骨科外固定器械仿生结构合理性评价。
- 上一篇:高分散性生物基全降解热塑性淀粉TPS:可与PBAT、
- 下一篇:生物医用金属材料
